



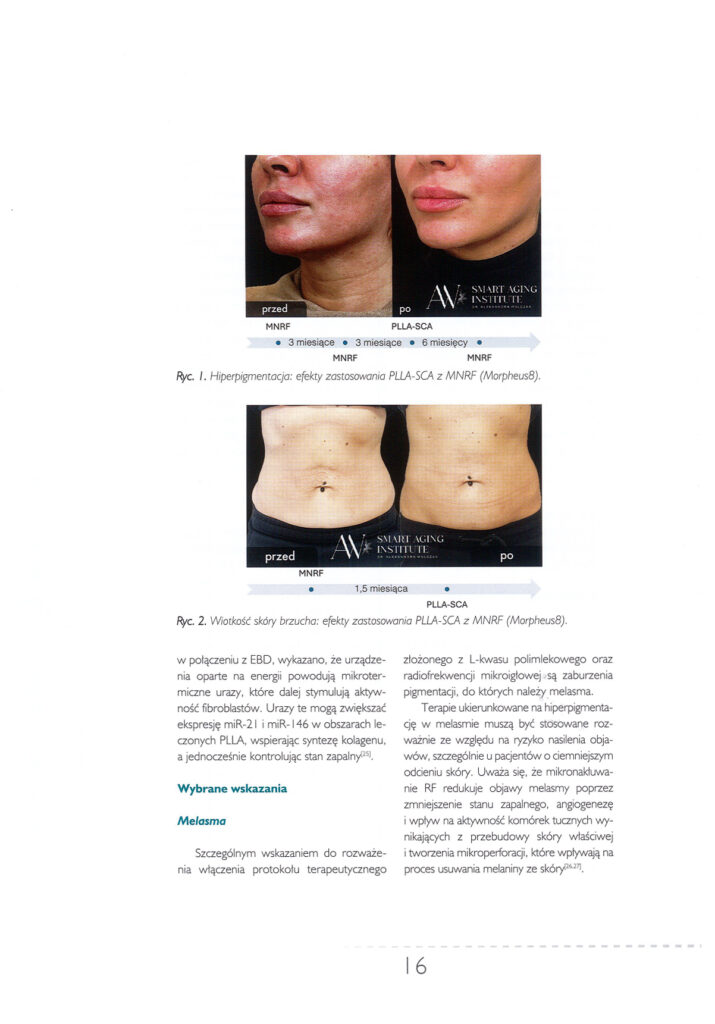


Synergia działania zabiegów opartych na wykorzystaniu kwasu L-polimlekowego (PLLA) oraz radiofrekwencji mikroigłowej (RFMN).
Dr n. med. Aleksandra Walczak
W gabinecie medycyny estetycznej Pacjenci coraz częściej decydują się na zabiegi, które przynoszą długotrwałe efekty. Działając w duchu założenia, że medycyna estetyczna pełni funkcję estetyczno-naprawczą, warto zwrócić uwagę nie tylko na kreowanie efektów poprawiających wygląd Pacjenta, ale także na działania służące działaniom skoncentrowanym na regeneracji. Co to dokładnie oznacza? Wśród zmian związanych z wiekiem wyróżniamy wiele mechanizmów, które prowadzą do degradacji tkanki i zmian w zakresie funkcjonowania komórek. O tych procesach wiemy coraz więcej, dlatego obecnie mamy możliwość nie tylko „zakamuflowania” tego, co uległo uszkodzeniu, ale realnie wpłynięciu na odbudowę opartą na regeneracji, a nawet profilaktyce dalszych zmian. Działanie w duchu longevity w obrębie skóry pozwala Pacjentom nie tylko wyglądać lepiej, ale także lepiej znosić zmiany przychodzące z wiekiem, a co za tym idzie – czuć się lepiej.
Jednym ze sposobów na optymalizację działania slow-aging jest łączenie kwasu L-polimlekowego (PLLA) z zabiegami wykorzystującymi urządzenia wysokiej energii tzw. EBD (Energy-based devices), wśród których na szczególną uwagę zasługuję technologia RFMN – Radiofrequency Microneedling.
Procesy starzenia w skórze i tkance podskórnej
Stopniowe zmniejszanie liczby komórek macierzystych i fibroblastów oraz ich nieefektywna funkcja prowadzi do zmian strukturalnych skóry, obejmujących m.in. degradację kolagenu, elastyny czy zmniejszenie ilości proteoglikanów (Goldie K., 2023; Shin SH, 2023). Starzejące się fibroblasty tworzą mikrośrodowisko sprzyjające procesom starzenia (Wlaschek M, 2021). W takim środowisku aktywacji ulegają metaloproteinazy (metalloproteinases, MMPs), które przyspieszają degradację macierzy pozakomórkowej (extracellular matrix, ECM) i hamują uwalnianie czynników wzrostu (Goldie K, 2023). Ponadto, w wyniku nieprawidłowego metabolizmu kolagenu i elastyny, powstają złożone pętle ujemnego sprzężenia zwrotnego, w efekcie których dochodzi do zwiększania ilości MMP i dalszej degradacji ECM (Goldie K., 2023, Shin JW., 2019). Powierzchowne i głębokie kompartmenty tłuszczowe także podlegają przemianom. Dodatkowo manifestem starzenia są zmiany, które zachodzą w obrębie kompartmentów tłuszczowych – tkanka tłuszczowa ulega repozycji, co staje się najbardziej widoczne w takich okolicach jak fałd nosowo-wargowy czy przestrzeń znajdująca się na wysokości linii żuchwy, bocznie od więzadła skórno-żuchwowego, w nomenklaturze anglosaskiej określana jako „jowl”
(w Polsce opisywana potocznie jako „chomiki”)( Swift A, 2021).
Zgodnie z najnowszymi doniesieniami, istotnym elementem związanym także z tkanką tłuszczową, odpowiedzialnym za prawidłową regeneracyjną funkcję tkanki, jest dermalna tkanka tłuszczowa dWAT (dermal white adipose tissue). Mechanizm,
za pomocą którego dWAT wspomaga gojenie się ran, można podzielić na następujące dwa procesy. Pierwszy następuje podczas wczesnej fazy krzepnięcia i stanu zapalnego
w przebiegu gojenia się ran. Shook BA wykazał, że dWAT, poprzez proces β-oksydacji lub lipolizy, wydziela trójglicerydy, aby regulować infiltrację makrofagów zapalnych, pomagając w inicjowaniu odpowiedzi immunologicznej (Shook et al., 2020a). Następny etap postępuje w miarę przechodzenia gojenia rany w fazę naprawy i przebudowy, dWAT ulega wówczas dedyferencjacji i przekształca się w komórki podobne do fibroblastów
i miofibroblasty. Komórki te przyczyniają się do budowy nowych struktur, które wspomagają gojenie, zapewniając regenerację tkanek na brzegach rany. (Zhang et al.,2019a)
Dodatkowo, w obrębie dermalnej tkanki tłuszczowej warto zwrócić uwagę na ADSC (adipose derived stem cells), czyli komórki mezenchymalne tkanki tłuszczowej, posiadające zdolność do różnicowania się i regeneracji. W odpowiedzi na stymulację ADSC mogą szybko wytwarzać cytokiny, hormony i czynniki wzrostu, co prowadzi do odbudowy skóry (Ridha Z, 2024). Badanie przeprowadzone przez Kima i wsp. (Kim WS, 2008) wykazało, że ADSC mają również działanie antyoksydacyjne na fibroblasty. Ochrona przed reaktywnymi formami tlenu (ang. ROS, reactive oxygen species) następuje prawdopodobnie dzięki cytokinom ochronnym i innym składnikom wytwarzanym przez ADSC, takimi jak IGF (insulin-like growth factor), który zapobiega uszkodzeniom oksydacyjnym fibroblastów. ADSC dodatkowo oddziałują na fibroblasty, stymulując ich migrację, wyzwalając produkcję kolagenu i wspomagając gojenie się ran i odmładzanie skóry.
Zatem, dobierając zabiegi do protokołów łączonych warto zwrócić uwagę na to, aby ich działania przynosiły synergistyczne efekty w zakresie regeneracji. Bazując na informacjach dotyczących dermalnej tkanki tłuszczowej, która pełni funkcje nie objętościowe, a stricte regeneracyjne oraz zdolności do różnicowania w odpowiedzi na działania bodźca uszkadzającego, możemy dojść do konkluzji, że stymulacja mechaniczna z komponentą termalną na odpowiedniej głębokości pozwala uzyskać optymalne dla nas i Pacjentów rezultaty. Odpowiednio dobrana pozwala na redukcję tkanki tłuszczowej w warstwie podskórnej i stymulację składowych warstwy dWAT
w warstwie skóry właściwej, w tym komórek macierzystych, pobudzając szlaki regeneracyjne tkanek.
Mechanizm działania PLLA
Kwas L-polimlekowy (w niniejszej pracy opisywany PLLA-SCA) jako substancją syntetyczną, biokompatybilną i jako produkt występuje w postaci liofilizowanego proszku z mikrocząsteczkami PLLA-SCA, mannitolem i karboksymetylocelulozą sodową. Gotowy produkt do iniekcji przygotowuje się go w postaci zawiesiny przy użyciu sterylnej wody
do wstrzykiwań. (Vleggaar D, 2014)
Biokompatybilne, polimerowe biomateriały, takie jak PLLA, po zaimplementowaniu wywołują reakcję ciała obcego, zależną od charakterystyki materiału, specyfiki pacjenta i techniki iniekcji. Kontrolowanie tych czynników zapewnia przewidywalną odpowiedź gospodarza, kluczową dla osiągnięcia pożądanych rezultatów zależnych od stymulacji kolagenu (Avelar L.E, 2025). Cząsteczki PLLA, które po iniekcji znajdują się w obrębie skóry właściwej otaczane są przez makrofagi, które przechodzą na fenotyp regeneracyjny, aktywnie uwalniając regeneracyjne cytokiny (Oh S, 2023). Następnie dochodzi
do aktywacji, migracji oraz proliferacji starzejących się fibroblastów (Oh S, 2023, Goldberg D, 2013). Działania te z czasem prowadzą do produkcji nowego kolagenu typu I i elastyny, niezbędnych do przebudowy macierzy pozakomórkowej (Oh S, 2023, Pfisterer K, 2021).
Ponadto, w wyniku działania kwasu L-polimlekowego dochodzi do wzrostu ekspresji lamininy i proteoglikanów oraz zwiększonej regulacji integryny, co prowadzi do lepszego przekazywania sygnałów pomiędzy tkanką podskórną, skórą właściwą a naskórkiem (Pfisterer K, 2021, Huth S, 2024). PLLA wpływa także na przekształcenie progenitorowych komórek tłuszczowych w dojrzałe adipocyty, przywracając jędrność skóry (Kim HW 2023, Trevor LV, 2020).
Radiofrekwecnja mikroigłowa
Radiofrekwencja mikroigłowa (RFMN) to zabieg należący do grupy zabiegów EBD, dający efekt odmłodzenia skóry, który łączy w sobie mechaniczne uszkodzenia skóry wywołane penetracją mikroigieł oraz ciepło wytwarzane przez fale radiowe. (Alexiades M. 2020). Radiofrekwencja może oddziaływać na kolagen w głębokich warstwach skóry
i podwyższać temperaturę skóry właściwej poprzez efekt przewodzenia ciepła pola elektrycznego o wysokiej częstotliwości. Po podgrzaniu tkanki dochodzi do szeregu zmian fizycznych i chemicznych, których celem jest stymulowanie procesów ukierunkowanych na regenerację i przebudowę kolagenu, co daje efekt napięcia skóry. (Bogle MA, 2007, Wu X, 2024)
Fale radiowe są chromoforoniezależne i mogą dostarczać energię do skóry właściwej
ze zdecydowanie zredukowanym ryzykiem wystąpienia pozapalnej hiperpigmentacji wynikającej z uszkodzenia naskórka, dlatego można je bezpiecznie stosować
w przypadku wszystkich typów skóry. (Dayan E. 2019, Dayan 2020)
Mikronakłuwanie RF umożliwia dostarczanie ciepła na zmiennej głębokości, co przekłada się na szeroki zakres lokalizacji anatomicznych i typów tkanek, które można skutecznie poddawać terapii. Mikronakłuwanie RF (Morpheus8, InMode Aesthetics) następuje
w formie frakcjonowanej, pozostawiając nienaruszone segmenty skóry rozproszone między segmentami poddawanymi terapii – jest to celowe działanie służące skróceniu czasu gojenia. Wywołanie mikrouszkodzeń skóry pobudza nowotworzenie kolagenu, elastyny i naczyń krwionośnych, co skutkuje obkurczaniem się i pogrubieniem warstwy skóry właściwej (Dayan 2019, Weiner SF, 2019).
Zazwyczaj docelowym progiem jest osiągnięcie co najmniej 500 impulsów podczas wykonywania zabiegów w obrębie twarzy; jednak u pacjentów ze znacznym nasileniem wiotkości i obecnością zmarszczek, ale dobrze tolerujących zabieg, takim progiem docelowym może być nawet 1000 impulsów. Z naukowego i klinicznego punktu widzenia, optymalnym rozwiązaniem jest wykonywanie zabiegu na kilku głębokościach (1-3 mm), aby najskuteczniej wpłynąć na jakość skóry. (Hendricks, 2022)
Połączenie obu zabiegów – aspekt naukowy
W doświadczeniach przeprowadzonych przez Wu et al. zbadano połączenie PLLA z RFMN u 32 osób leczonych z objawami wiotkości skóry twarzy. Badanie wykazało znaczną poprawę wiotkości skóry, ze wzrostem grubości skóry właściwej (Wu X, 2023). Ponadto, jako podłoże synergistycznych efektów PLLA w połączeniu z EBD wykazano,
że urządzenia oparte na energii powodują mikrotermiczne urazy, które dalej stymulują aktywność fibroblastów. Urazy te mogą zwiększać ekspresję miR-21 i miR-146
w obszarach leczonych PLLA, wspierając syntezę kolagenu, jednocześnie kontrolując stan zapalny (Byun KA, 2024).
Wybrane wskazania:
Melasma
Szczególnym wskazaniem do rozważenia włączenia protokołu terapeutycznego złożonego z L-kwasu polimlekowego oraz radiofrekwencji mikroigłowej są zaburzenia pigmentacji, do których należy melasma.
Terapie ukierunkowane na hiperpigmentację w melasmie muszą być stosowane rozważnie ze względu na ryzyko nasilenia objawów, szczególnie u pacjentów
o ciemniejszym odcieniu skóry. Uważa się, że mikronakłuwanie RF redukuje objawy melasmy poprzez zmniejszenie stanu zapalnego, angiogenezę i wpływ na aktywność komórek tucznych wynikających z przebudowy skóry właściwej i tworzenia mikroperforacji, które wpływają na proces usuwania melaniny ze skóry (Tan MG, 2021, Jung JW., 2019).
Ryc.1
3xRF à PLLA-SCA
Udowodniono, że kwas L-polimlekowy PLLA-SCA wpływa na ekspresję genów związanych z procesami regeneracji, takich jak HGF (różnicowanie komórek pluripotencjalnych) czy DKK-1 (regulacja pigmentacji) (Weibel J, 2025).
Połączeniu obu zabiegów w jednym protokole leczniczym u pacjentów z objawami hiperpigmentacji przynosi satysfakcjonujące rezultaty w postaci wyrównania kolorytu skóry (Ryc. 1). Na zdjęciu (Ryc. 1, zdjęcia z prywatnej praktyki) widoczne są efekty zabiegowe uzyskane u Pacjentki, u której 3-krotnie wykonano zabieg z użyciem radiofrekwencji mikroigłowej w odstępie dwóch miesięcy (InMode Morpheus8),
a następnie wykonano zabieg biostymulująco-regeneracyjny z użyciem kwasu L-polimlekowego (PLLA-SCA, Sculptra, rekonstytuowany w 8 mL aqua pro injectione, 2 mL 1% lidokainy) po upływie dwóch miesięcy. Widoczna jest redukcja zmian hiperpigmentacyjnych oraz poprawa napięcia skóry.
Konturowanie ciała
Szczególnie wartościową cechą zabiegu RFMN jest możliwość adresowania różnych głębokości podczas zabiegu pozwala na redukcję tkanki tłuszczowej z jednoczesnym wpływem na obkurczenie i stymulację skóry właściwej (InMode Aesthetics, 2022). Taki model działania pozwala na uzyskanie efektów lipolitycznych bez obawy o nasilenie wiotkości skóry.
U Pacjentki widocznej na zdjęciu (Ryc. 2 ) zastosowano protokół terapeutyczny, składający się z pojedynczego zabiegu RFMN (InMode Morpheus8; działanie na głębokościach: 6, 5, 4, 3 oraz 2 mm) oraz zabiegu z wykorzystaniem kwasu L-polimlekowego (PLLA-SCA, Sculptra, rekonstytuowany w 18 mL aqua pro injectione, 2 mL 1% lidokainy) w odstępie 1,5 miesiąca. Zastosowanie obu zabiegów pozwoliło na poprawę jakości skóry i poprawę jej napięcia.
Ryc. 2

1xRF à 1xPLLA
PODSUMOWANIE
Synergia działania procedur zabiegowych o zróżnicowanym profilu działania pozwala na uzyskanie jeszcze lepszych efektów i/lub w krótszym czasie. Przykładem takiego efektywnego połączenia jest zastosowanie radiofrekwencji mikroigłowej w połączeniu
z kwasem L-polimlekowym w odpowiednim odstępie czasu.
Wykorzystanie bodźca termalnego na poziomie tkanki podskórnej pozwala na redukcję tkanki tłuszczowej w okolicach, które charakteryzują się jej nadmiarem, czego przykładem mogą być powierzchowne kompartmenty tłuszczowe w obrębie podbródka, lub – wspomniane wcześniej okolice „jowls”, wynikające z repozycji tkanek. Działanie na poziomie skóry właściwej może prowadzić do stymulacji składowych warstwy dWAT,
w tym komórek macierzystych, pobudzając szlaki regeneracyjne tkanek. Ponadto obie metody prowadzą do neokolagenezy i neoelastogenezy, które determinują przebudowę tkanki. Neoangiogeneza wywołana działaniem radiofrekwencji oraz wzmożona ekspresja białek odpowiedzialnych za integralność tkanki czy jej pigmentację, wywołana działaniem PLLA-SCA, przekładają się na korzystne efekty zabiegowe pod postacią m.in. poprawy napięcia skóry i wyrównania kolorytu.
…
BIBLIOGRAFIA
Alexiades M. Microneedle radiofrequency. Facial Plast Surg Clin North Am. 2020;28:9-15
Avelar, L.E., Nabhani, S. and Wüst, S. (2025), Unveiling the Mechanism: Injectable Poly-L-Lactic Acid’s Evolving Role—Insights From Recent Studies. J Cosmet Dermatol, 24: e16635.
Bogle MA, Ubelhoer N, Weiss RA, Mayoral F, Kaminer MS. Evaluation of the multiple pass, low fluence algorithm for radiofrequency tightening of the lower face. Lasers Surg Med. 2007;39:210–217.
Dayan E, Chia C, Burns AJ, Theodorou S. Adjustable depth fractional radiofrequency combined with bipolar radiofrequency: a minimally invasive combination treatment for skin laxity. Aesthet Surg J. 2019;39(Suppl_3):S112- S119.
Dayan E, Burns AJ, Rohrich RJ, Theodorou S. The use of radiofrequency in aesthetic surgery. Plast Reconstr Surg Glob Open. 2020;8(8):e2861.
InMode Aesthetics. Morpheus8. 2022. Accessed February 05,
2022. https://www.inmod emd.co.uk/morph eus8
W.S. Kim, B.S. Park, H.K. Kim, J.S. Park, K.J. Kim, J.S. Choi, S.J. Chung, D.D. Kim, J.H. Sung, Evidence supporting antioxidant action of adipose-derived stem cells: protection of human dermal broblasts from oxidative stress. J. Dermatol. Sci. 49, 133–142 (2008).
Oh S, Lee JH, Kim HM et al (2023) Poly-L-lactic acid fillers improved dermal collagen synthesis by modulating M2 macrophage polarization in aged animal skin. Cells.
Byun K-A, Lee JH, Lee SY et al (2024) Piezo1 activation drives enhanced collagen synthesis in aged animal skin induced by poly L-lactic acid fillers. Int J Mol Sci 25:7232.
Hendricks AJ, Farhang SZ. Dermatologic facial applications of Morpheus8 fractional radiofrequency microneedling. J Cosmet Dermatol. 2022 Oct;21 Suppl 1:S11-S19. doi: 10.1111/jocd.15231. Epub 2022 Aug 2.
Shook, B. A., Wasko, R. R., Mano, O., Rutenberg-Schoenberg, M., Rudolph, M. C.,Zirak, B., et al. (2020a). Dermal adipocyte lipolysis and myofibroblast conversion are required for efficient skin repair. Cell. Stem Cell. 26 (6), 880–895.
D. Vleggaar, R. Fitzgerald, and Z. P. Lorenc, “Composition and Mechanism of Action of Poly- L- Lactic Acid in Soft Tissue Augmentation,” Journal of Drugs in Dermatology 13, no. 4 Suppl (2014): s29–s31.
Z. Ridha, S.G. Fabi, R. Zubair, S.H. Dayan. Decoding the implications of glucagon-like peptide-1 receptor agonists on accelerated 4 facial and skin aging. Aesthet. Surg. J. (2024).
Weiner SF. Radiofrequency microneedling: overview of technol-
ogy, advantages, differences in devices, studies, and indications.
Facial Plast Surg Clin North Am. 2019;27(3):291- 303.
Zhang, Z., Shao, M., Hepler, C., Zi, Z., Zhao, S., et al. (2019a). Dermal adipose tissue
has high plasticity and undergoes reversible dedifferentiation in mice. J. Clin. Investig.
129 (12), 5327–5342.
Oh S, et al. Antioxidants (Basel). 2023;12(6):1204;
Goldberg D, et al. Dermatol Surg. 2013;39(6):915–922;
Pfisterer K, et al. Front Cell Dev Biol. 2021;9:682414. Publikacja 6 lipca 2021 r.;
Huth, S et al. J Drugs Dermatol. 1 kwietnia 2024 r.;23(4):285-288;
Kim HW, et al. Ann Dermatol. 2023;35(6):424-431;
Trevor LV, et al. J Clin Med. 2020;9(7):2161. Publikacja 8 lipca 2020 r.
Wu X, Cen Q, Wang X et al (2023) Microneedling radiofrequency enhances poly-L-lactic acid penetration that effectively improves facial skin laxity without lipolysis. Plast Reconstr Surg.
Tan MG, Jo CE, Chapas A, Khetarpal S, Dover JS. Radiofrequency microneedling: a comprehensive and critical review. Dermatol Surg. 2021;47(6):755- 761.
Jung JW, Kim WO, Jung HR, Kim SA, Ryoo YW. A face- split study to evaluate the effects of microneedle radiofrequency with Q-switched Nd:YAG laser for the treatment of melasma. Ann Dermatol. 2019;31(2):133- 138.
Waibel J, Nguyen TQ, Le JHTD, Qureshi A, Ziegler M, Widgerow A, Meckfessel M. Gene Analysis of Biostimulators: Poly-L-Lactic Acid Triggers Regeneration While Calcium Hydroxylapatite Induces Inflammation Upon Facial Injection. J Drugs Dermatol. 2025 Jan 1;24(1):34-40.
Goldie K. The evolving field of renerative aesthetics. J Cosmet Dermatol. 2023;22 Suppl 1:1-7.
Shin SH, Lee YH, Rho NK et al. Skin aging from mechanisms to interventions: focusing on dermal aging. Front Physiol. 2023;14:1195272.
Wlaschek M, Maity P, Makrantonaki E, et al. Connective tissue and fibroblast senescence in skin aging. J Invest Dermatol. 2021;141:985-92.
Shin JW., Kwon SH, Choi jY, et al. Molecular mechanisms of dermal aging and antiaging approaches. Int J Mol Sci. 2019;20.
Swift A, Liew S, Weinkle S, et al. The facial aging process from the „Inside Out”. Aesthet Surg J. 2021; 41:1107-1119.


